Anvisa diz que aguarda resposta sobre pendências em pedido da Fiocruz
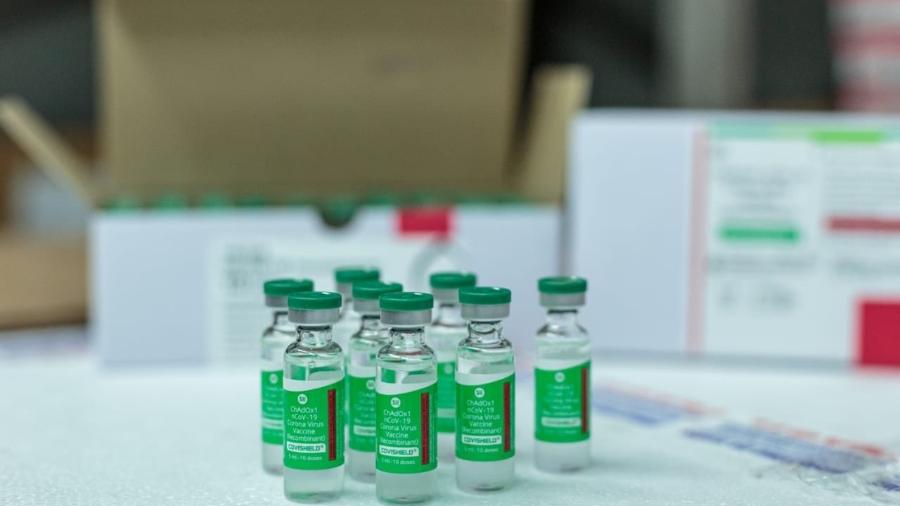
A Anvisa (Agência Nacional de Vigilância Sanitária) deu atualizações hoje sobre como anda o pedido de registro definitivo da vacina contra a covid-19 da AstraZeneca/Oxford, que foi feito pela Fiocruz (Fundação Oswaldo Cruz). Segundo a agência federal, o processo aguarda ainda a resposta sobre pendências apontadas pela Anvisa para chegar a um parecer final.
A explicação foi dada no dia em que Anvisa concedeu o registro de uso definitivo para a vacina da Pfizer/Biontech, o primeiro do tipo no país. A autorização foi definida 18 dias após a entrada do pedido. Já a solicitação da Fiocruz, que produzirá a vacina de Oxford no Brasil, foi feita uma semana antes, em 29 de janeiro.
"A gente fez uma reunião com eles semana passada e existem ainda informações que precisam ser complementadas. A gente precisa ter dados da vacina fabricada aqui no Brasil porque o pedido pressupõe essa fabricação aqui, e como ainda estão no processo de fabricação, a gente solicitou a complementação e agora está na pendência deles", disse o gerente-geral de medicamentos da Anvisa, Gustavo Mendes.
Profissionais da agência federal concederam entrevista coletiva hoje em Brasília para detalhar o processo que levou à aprovação do primeiro registro definitivo de uma vacina contra a covid-19 no país. Com a autorização, o imunizante da Pfizer pode ser aplicado não apenas em grupos prioritários, como vem sendo feito com a CoronaVac e a vacina de Oxford, mas também para a população em geral.
O tempo de conclusão do pedido da Pfizer impressionou por ser bem mais curto do que o usual praticado pela Anvisa, de 60 dias, e o anúncio de hoje não era esperado. O contexto levou a um questionamento na entrevista coletiva se o imunizante da Pfizer não teria sido priorizado na análise da Anvisa.
"De forma alguma, na verdade o da AstraZeneca já vinha [sendo analisado] pelo processo de submissão contínua. O da Pfizer acabou sendo mais rápido por questões circunstanciais, porque quando a Pfizer submeteu - a gente sempre faz reuniões e sempre sabe o que a empresa vai submeter -, a gente sabia que no caso da Pfizer teria mais informações do que da AstraZeneca", explicou Mendes.
"Então já era esperado que houvesse um tempo maior de análise, até pela empresa [AstraZeneca]", completou o gerente da Anvisa.













ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.